Upaya pengendalian Penyakit Tuberkulosis dengan menggunakan strategi DOTS (Directly Observed Treatment Short-course) dengan 5 komponennya, yaitu :
Komitmen politis, dengan peningkatan dan kesinambungan pendanaan.
Penemuan kasus melalui pemeriksaan dahak mikroskopis yang terjamin mutunya.
Pengobatan yang standar, dengan supervisi dan dukungan bagi pasien.
Sistem pengelolaan dan ketersediaan OAT yang efektif.
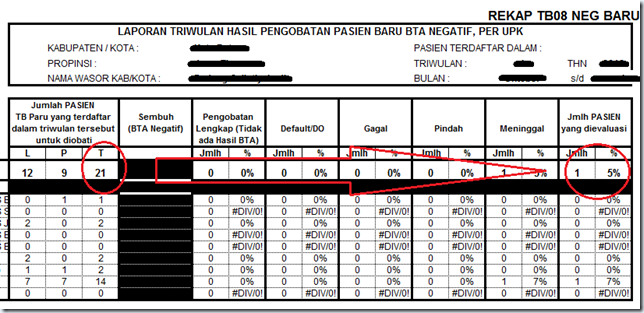
Sistem monitoring pencatatan dan pelaporan yang mampu memberikan penilaian terhadap hasil pengobatan pasien dan kinerja program.
Komponen yang kedua : Penemuan kasus melalui pemeriksaan dahak mikroskopis yang terjamin mutunya, ini sangat berkaitan erat dengan mutu laboratorium di fasilitas pelayanan kesehatan. Laboratorium untuk pemeriksaan dahak sangat menentukan dalam mendiagnosis pada suspek TB. Mutu kinerja laboratorium mikroskopis TB dilakukan melalui pelaksanaan Pemantapan Mutu Eksternal (PME) dengan melakukan Uji Silang sediaan BTA oleh Laboratorium Rujukan Uji Silang (RUS) dalam jejaring laboratorium di wilayah.
Selama ini Uji Silang sediaan BTA dilakukan dengan metode konvensional yaitu 100% sediaan positif ditambah 10% sediaan negatif dengan Error Rate <5%. Mulai tahun 2007 Ditjen P2&ML Kemenkes RI telah melakukan Workshop tentang Uji Silang dengan metode LQAS (Lot Quality Assurance Sampling) di beberapa wilayah di Indonesia. Hasil dari workshop tersebut mulai diterapkan pada tahun 2009.
Perbedaan Uji Silang Metode Konvensional dengan LQAS :
Konvensional |
LQAS |
Samping : 100% slide positif ditambah 10% slide negatif |
Samping : semua slide mendapat kesempatan yang sama |
Pemilihan slide tergantung dari minat petugas |
Pemilihan secara acak dengan menggunakan statistik sederhana |
Formulir TB05, TB04 dan TB12 |
Formulir TB05, TB04 dan TB12 yang disempurnakan |
Penyimpanan dipisahkan antara slide positif dan negatif |
Penyimpanan slide digabung sesuai dengan TB04 |
Analisis Uji Silang adalah Error Rate |
Berdasarkan derajat kesalahan |
Error Rate >5% = jelek |
Satu Kesalahan Besar atau tiga Kesalahan Kecil = jelek |
Kualitas : Sediaan dan Pewarnaan |
Kualitas : Spesimen, Pewarnaan, Kebersihan, Ketebalan, Ukuran dan Kerataan |
Dengan adanya Metode LQAS ini :
- Tidak mengubah sistem uji silang tetapi hanya memutakhirkan metode uji silang.
- Menilai kinerja laboratorium secara menyeluruh.
- Tidak untuk konfirmasi diagnosis.
- Sediaan disimpan berdasarkan TB04.
- Setiap sediaan memelikik kesempatan yang sama untuk di uji silang.
- Penilaian kinerja berdasarkan jumlah dan tipe kesalahan bukan prosentase.
- Kemungkinan penyebab kesalahan lebih mudah diketahui.
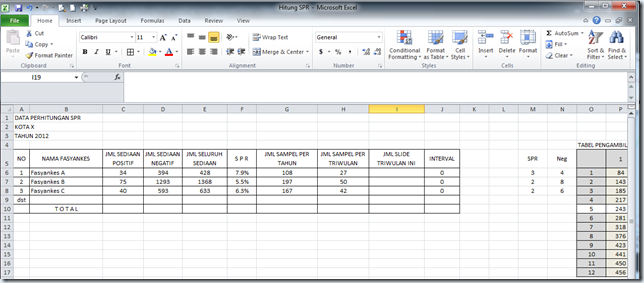
Langkah-langkah dalam melakukan metode uji silang LQAS:
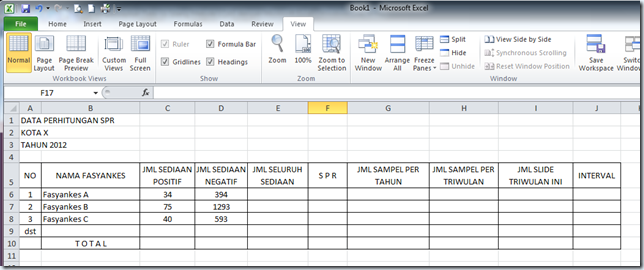
- Tentukan jumlah seluruh sediaan, jumlah sediaan positif dan jumlah sediaan negatif yang diperiksa pada tahun lalu.
Nama Fasyankes |
Total Sediaan |
Jumlah Sediaan Positif |
Jumlah Sediaan Negatif |
A |
428 |
34 |
394 |
B |
1368 |
75 |
1293 |
C |
633 |
40 |
593 |
Hitung Slide Positivity Rate (SPR). SPR = Proporsi sediaan Positif diantara seluruh sediaan.
Nama Fasyankes |
Total Sediaan |
Jumlah Sediaan |
S P R |
A |
394 |
34 |
7,9% |
B |
1293 |
75 |
5,5% |
C |
593 |
40 |
6,3% |
Tentukan Sensitifitas, spesifitas dan jumlah kesalahan yang dapat diterima. Program P2TB menetapkan Sensitifitas=80%, Spesifitas=100% dan Jumlah Kesalahan yang dapat diterima=0.
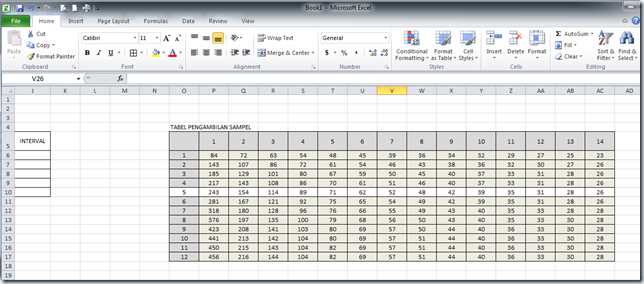
Pembacaan tabel pengambilan sediaan untuk metode LQAS. SPR
dibulatkan ke angka terdekat, Jumlah sediaan negatif
dibulatkan ke angka terdekat. 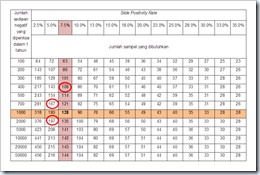
Hitung Jumlah Sediaan Uji Silang. Fasyankes A dengan SPR = 7,9% dibulatkan menjadi 7,5%, jumlah sediaan negatif 394 dibulatkan menjadi 400. Lihat perpotongan antara SPR 7,5% dan Sediaan negatif 400 yaitu 108 (untuk jumlah sediaan yang di uji silang selama 1 tahun). Untuk Fasyankes B
jumlah sediaan yang di uji silang = 197, Fasyankes C = 167. Bila jumlah sediaan dalam 1 tahun kurang dari jumlah sampel maka seluruh sediaan yang ada harus diambil untuk uji silang.
Hitung jumlah sediaan per triwulan. Jumlah sediaan yang sesuai dengan perpotongan (langkah 5) dibagi 4. Misalnya Fasyankes A, jumlah sediaan yang akan di uji silang = 108 dibagi 4 = 27. Jadi jumlah sediaan per triwulan di Fasyankes A yang akan di uji silang sebanyak 27 slide. Bila pada triwulan tersebut jumlah sediaan kurang maka seluruh sediaan di uji silang. Hasil pembagian per triwulan dibulatkan ke atas.
Hitung interval pengambilan sediaan. Pada langkah ini memerlukan data jumlah seluruh sediaan pada triwulan yang akan dilakukan uji silang sesuai dengan TB04. Misalnya jumlah seluruh sediaan pada triwulan yang akan di uji silang sebanyak 200 slide, maka 200 dibagi 27 = 7,407 dan dibulatkan ke atas menjadi 8. Jadi interval untuk Fasyankes A = 8.
Tentukan pengambilan sediaan pertama (Lot). Penentuan sediaan yang akan diambil pertama harus lebih kecil atau sama dengan interval. Misalnya interval 8, maka yang diambil adalah 1 slide diantara slide nomor 1 sampai slide nomor 8.

Pengambilan sediaan berdasarkan interval dan sesuai urutan TB04. Misalnya slide pertama yang diambil adalah slide nomor 5, maka sediaan yang akan di uji silang nomor : 5,13,21,29,37,45,53,61,69,85,93,101,109,117,125,133,141, 149,157,165,173,181,189,197. Jika ada salah satu slide hilang atau pecah, misal slide nomor 61 hilang maka slide nomor 61 diganti slide nomor 62. Urutan selanjutnya tetap.
KLASIFIKASI KESALAHAN BACA
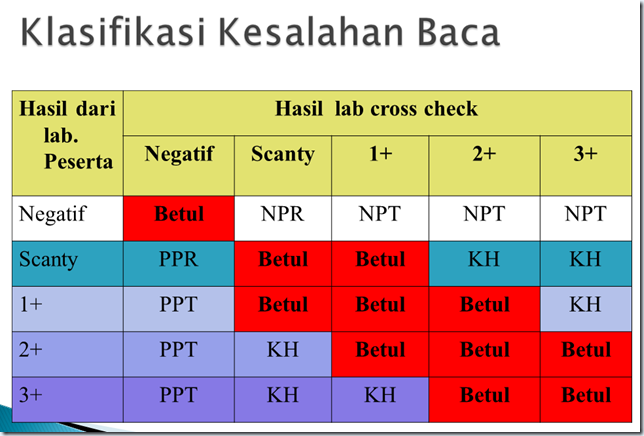
KB = Kesalahan Besar
KK = Kesalahan Kecil
NPT = Negatif Palsu Tinggi
PPR = Positif Palsu Rendah
KH = Kesalahan Hitung
PPT = Positif Palsu Tinggi
Penilaian Kinerja Laboratorium dikatakan JELEK jika :
- Terdapat KB (PPT, NPT).
- Terdapat 3 KK yang nilainya setara dengan 1 KB.
Dengan adanya Uji Silang LQAS diharapkan mutu kinerja Laboratorium Pemeriksaan Tuberkulosis akan semakin terjamin dan memberikan kemudahan bagi pengelola program dalam melakukan analisa.
 Perhatikan nomor rows, pada keadaan filter angka berwarna biru
Perhatikan nomor rows, pada keadaan filter angka berwarna biru